آلبرت انیشتین از کوانتا برای توضیح اثر فوتوالکتریک استفاده می کند
[ ویرایش ]
مقاله اصلی: اثر فوتوالکتریک
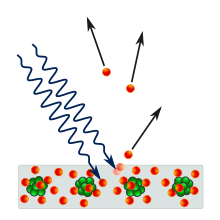
نور از سمت چپ به سطح می تابد. اگر فرکانس نور به اندازه کافی زیاد باشد، یعنی اگر انرژی کافی ارائه کند، الکترون های دارای بار منفی از فلز خارج می شوند.
در سال 1887، هاینریش هرتز مشاهده کرد که وقتی نور با فرکانس کافی به سطح فلزی برخورد می کند، سطح اشعه کاتدی ساطع می کند . [ 1 ] : I:362 ده سال بعد، جی جی تامسون نشان داد که بسیاری از گزارشات از پرتوهای کاتدی در واقع "جسم" هستند و به سرعت الکترون نامیده می شوند . در سال 1902، فیلیپ لنارد کشف کرد که حداکثر انرژی ممکن یک الکترون پرتاب شده با شدت آن ارتباطی ندارد . [ 12 ] این مشاهدات در تضاد با الکترومغناطیس کلاسیک است، که پیش بینی می کند انرژی الکترون باید متناسب با شدت تابش فرودی باشد. [ 13 ] : 24
آلبرت انیشتین ج. 1905
در سال 1905، آلبرت انیشتین پیشنهاد کرد که حتی اگر مدلهای پیوسته نور برای پدیدههای نوری میانگین زمانی بسیار خوب عمل میکنند، برای انتقالهای لحظهای انرژی در نور ممکن است تعداد محدودی از کوانتومهای انرژی رخ دهد. [ 14 ] انیشتین از بخش مقدمه مقاله کوانتومی خود در مارس 1905 "درباره دیدگاه اکتشافی در مورد گسیل و تبدیل نور" می گوید:
طبق فرضی که در اینجا باید در نظر گرفت، وقتی یک پرتو نور از یک نقطه پخش می شود، انرژی به طور پیوسته در فضاهای در حال افزایش توزیع نمی شود، بلکه شامل تعداد محدودی از "کوانتوم های انرژی" است که در نقاطی از فضا قرار دارند. بدون تقسیم حرکت می کند و فقط به صورت کلی می تواند جذب یا تولید شود.
این جمله انقلابی ترین جمله نوشته شده توسط یک فیزیکدان قرن بیستم نامیده شده است. [ 15 ] انرژی یک کوانتوم نور فرکانسf

انیشتین فرض میکرد که یک کوانتای نوری تمام انرژی خود را به یک الکترون منتقل میکند و حداکثر انرژی hf را به الکترون میدهد. بنابراین، تنها فرکانس نور حداکثر انرژی قابل انتقال به الکترون را تعیین می کند. شدت تابش نور متناسب با شدت پرتو نور است. [ 14 ]
انیشتین استدلال کرد که برای حذف یک الکترون از فلز، مقدار معینی انرژی به نام تابع کار و با φ نشان داده می شود. [ 16 ] این مقدار انرژی برای هر فلز متفاوت است. اگر انرژی کوانتای نور کمتر از تابع کار باشد، انرژی کافی برای حذف الکترون از فلز را ندارد. فرکانس آستانه، f 0 ، فرکانس کوانتای نوری است که انرژی آن برابر با تابع کار است:
اگر f بزرگتر از f 0 باشد ، انرژی hf برای حذف یک الکترون کافی است. الکترون پرتاب شده دارای انرژی جنبشی E k است که حداکثر برابر با انرژی نور منهای انرژی لازم برای جدا کردن الکترون از فلز است:
توصیف انیشتین از نور به عنوان متشکل از کوانتوم های انرژی، مفهوم پلانک از انرژی کوانتیزه شده را گسترش داد، که این است که یک کوانتوم منفرد با فرکانس معین، f ، مقدار ثابتی از انرژی، hf را ارائه می دهد . در طبیعت به ندرت با تک کوانتوم ها مواجه می شویم. خورشید و منابع انتشار موجود در قرن نوزدهم در هر ثانیه مقدار زیادی انرژی ساطع می کنند. ثابت پلانک ، h ، آنقدر کوچک است که مقدار انرژی در هر کوانتوم، hf بسیار بسیار کم است. نوری که میبینیم شامل تریلیونها چنین کوانتایی است.
کوانتیزاسیون ماده: مدل بور اتم
[ ویرایش ]
مقاله اصلی: مدل بور
در سپیده دم قرن بیستم، شواهد نیاز به مدلی از اتم با ابری پراکنده از الکترونهای با بار منفی داشت که یک هسته کوچک، متراکم و با بار مثبت را احاطه کرده بود . این ویژگیها مدلی را پیشنهاد میکنند که در آن الکترونها مانند سیاراتی که به دور یک ستاره میچرخند، دور هسته میچرخند. مدل کلاسیک اتم، مدل سیارهای یا گاهی مدل رادرفورد نامیده میشود - پس از ارنست رادرفورد که آن را در سال 1911 بر اساس آزمایش ورقههای طلای گایگر-مارسدن پیشنهاد کرد ، که برای اولین بار وجود هسته را نشان داد. با این حال، همچنین شناخته شده بود که اتم در این مدل ناپایدار خواهد بود: طبق تئوری کلاسیک، الکترونهای در حال چرخش تحت شتاب مرکزگرا هستند و بنابراین باید تابش الکترومغناطیسی ساطع کنند، از دست دادن انرژی نیز باعث میشود که آنها به سمت هسته حرکت کنند و با هم برخورد کنند. با آن در کسری از ثانیه
دومین معمای مرتبط، طیف گسیل اتم ها بود. هنگامی که گاز گرم می شود، فقط در فرکانس های گسسته نور می دهد. برای مثال، نور مرئی ساطع شده توسط هیدروژن از چهار رنگ مختلف تشکیل شده است، همانطور که در تصویر زیر نشان داده شده است. شدت نور در فرکانس های مختلف نیز متفاوت است. در مقابل، نور سفید از انتشار پیوسته در سراسر طیف فرکانس های مرئی تشکیل شده است. در پایان قرن نوزدهم، یک قانون ساده به نام فرمول بالمر نشان داد که فرکانس خطوط مختلف چگونه با یکدیگر مرتبط است، البته بدون توضیح دلیل این امر، یا هیچ گونه پیش بینی در مورد شدت. این فرمول همچنین خطوط طیفی اضافی را در نور فرابنفش و مادون قرمز پیشبینی میکرد که در آن زمان مشاهده نشده بود. این خطوط بعداً به صورت تجربی مشاهده شدند و اعتماد به ارزش فرمول را افزایش دادند.
طیف انتشار هیدروژن هنگامی که برانگیخته می شود، گاز هیدروژن نور را در چهار رنگ متمایز (خطوط طیفی) در طیف مرئی و همچنین تعدادی خطوط در مادون قرمز و ماوراء بنفش منتشر می کند.
نشان می دهد
فرمول ریاضی که طیف انتشار هیدروژن را توصیف می کند
در سال 1905، آلبرت اینشتین از نظریه جنبشی برای توضیح حرکت براونی استفاده کرد . فیزیکدان فرانسوی ژان باپتیست پرین از این مدل در مقاله انیشتین برای تعیین تجربی جرم و ابعاد اتم ها استفاده کرد و بدین ترتیب تأیید تجربی مستقیم نظریه اتمی را ارائه کرد. [ نیازمند منبع ]
مدل کوانتومی اتم هیدروژن نیلز بور در سال 1913.
در سال 1913، نیلز بور مدل جدیدی از اتم را پیشنهاد کرد که شامل مدارهای الکترونی کوانتیزه شده بود: الکترونها همچنان مانند سیارهها به دور خورشید به دور هسته میچرخند، اما آنها مجاز هستند فقط در مدارهای خاصی زندگی کنند، نه اینکه در هر فاصله دلخواه به مدار بچرخند. [ 18 ] هنگامی که یک اتم انرژی ساطع کرد (یا جذب کرد)، الکترون در یک مسیر پیوسته از یک مدار به دور هسته به مدار دیگر حرکت نکرد، همانطور که به طور کلاسیک انتظار می رود. در عوض، الکترون فوراً از مداری به مدار دیگر می پرد و نور ساطع شده را به شکل فوتون منتشر می کند. [ 19 ] انرژیهای احتمالی فوتونهایی که توسط هر عنصر منتشر میشوند، با تفاوت در انرژی بین مدارها تعیین میشوند، و بنابراین طیف گسیل برای هر عنصر شامل تعدادی خط میشود. [ 20 ]
نیلز بور در جوانی
با شروع تنها از یک فرض ساده در مورد قاعده ای که مدارها باید از آنها پیروی کنند، مدل بور توانست خطوط طیفی مشاهده شده در طیف گسیل هیدروژن را به ثابت های شناخته شده قبلی مرتبط کند. در مدل بور، الکترون اجازه نداشت به طور مداوم انرژی ساطع کند و به هسته برخورد کند: هنگامی که در نزدیکترین مدار مجاز قرار گرفت، برای همیشه پایدار بود. مدل بور توضیح نداد که چرا مدارها باید به این روش کوانتیزه شوند، و همچنین قادر به پیشبینی دقیق برای اتمهای دارای بیش از یک الکترون، یا توضیح اینکه چرا برخی از خطوط طیفی درخشانتر از خطوط طیفی هستند، نبود.
برخی از مفروضات بنیادی مدل بور به زودی نادرست شدند - اما نتیجه کلیدی اینکه خطوط مجزا در طیف های گسیلی به دلیل برخی ویژگی های الکترون های اتم های در حال کوانتیزه شدن است، درست است. روشی که الکترونها در واقع رفتار میکنند با اتم بور و با آنچه ما در دنیای تجربیات روزمره خود میبینیم، به طرز چشمگیری متفاوت است. این مدل مکانیکی کوانتومی مدرن اتم در زیر مورد بحث قرار گرفته است .







 در این وبلاگ به ریاضیات و کاربردهای آن و تحقیقات در آنها پرداخته می شود. مطالب در این وبلاگ ترجمه سطحی و اولیه است و کامل نیست.در صورتی سوال یا نظری در زمینه ریاضیات دارید مطرح نمایید .در صورت امکان به آن می پردازم. من دوست دارم برای یافتن پاسخ به سوالات و حل پروژه های علمی با دیگران همکاری نمایم.در صورتی که شما هم بامن هم عقیده هستید با من تماس بگیرید.
در این وبلاگ به ریاضیات و کاربردهای آن و تحقیقات در آنها پرداخته می شود. مطالب در این وبلاگ ترجمه سطحی و اولیه است و کامل نیست.در صورتی سوال یا نظری در زمینه ریاضیات دارید مطرح نمایید .در صورت امکان به آن می پردازم. من دوست دارم برای یافتن پاسخ به سوالات و حل پروژه های علمی با دیگران همکاری نمایم.در صورتی که شما هم بامن هم عقیده هستید با من تماس بگیرید.