آنتروپی
قانون اول ترمودینامیک به انرژی خاصیت و بقای انرژی می پردازد. قانون دوم که در فصل قبل معرفی شد، منجر به تعریف خاصیت جدیدی به نام آنتروپی می شود. آنتروپی بر حسب یک عملیات حساب تعریف می شود و هیچ تصویر فیزیکی مستقیمی از آن نمی توان ارائه داد. در این فصل ابتدا نابرابری کلازیوس که مبنای تعریف آنتروپی است مورد بحث قرار خواهد گرفت. به دنبال آن بحث تغییرات آنتروپی که در طی فرآیندهای مختلف برای سیالات کاری مختلف رخ می دهد، خواهد بود. در نهایت، کار جریان ثابت برگشت پذیر و بازده ایزنتروپیک دستگاه های مهندسی مختلف مانند توربین و کمپرسور مورد بحث قرار خواهد گرفت.
نابرابری کلازیوس
همانطور که در شکل 5.1 نشان داده شده است، دو موتور حرارتی را در نظر بگیرید که بین دو مخزن در دمای T H و T L کار می کنند. از دو موتور حرارتی، یکی برگشت پذیر و دیگری غیر قابل برگشت است.
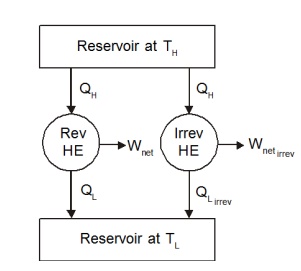
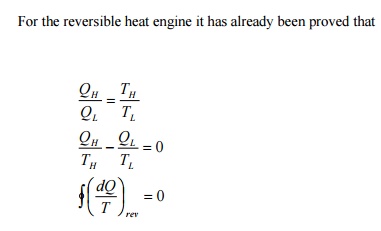
همانطور که قبلاً بحث شد، خروجی کار از موتور برگشت ناپذیر باید کمتر از موتور برگشت پذیر برای همان ورودی حرارت QH باشد . بنابراین Q L,Irrev بزرگتر از QL ,Rev خواهد بود . بیایید تعریف کنیم
QL,Irrev =QL,Rev +dQ
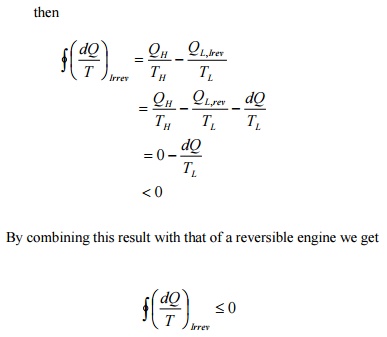
این به عنوان نابرابری کلازیوس شناخته می شود .
نابرابری کلازیوس مبنای تعریف خاصیت جدیدی است که به آنتروپی معروف است.
سیستمی را که از حالت 1 تا حالت 2 در امتداد یک مسیر برگشت پذیر A همانطور که در شکل 5.2 نشان داده شده است، در نظر بگیرید. اجازه دهید سیستم از حالت 2 در طول مسیر برگشت پذیر B به حالت اولیه 1 برگردد. اکنون سیستم یک چرخه را تکمیل کرده است. با اعمال نابرابری کلازیوس به دست می آوریم
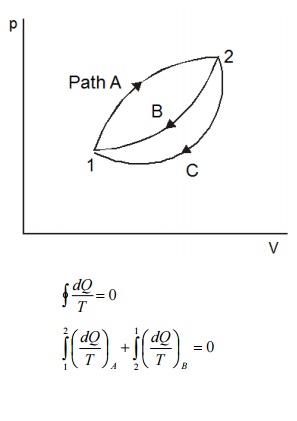
به جای اینکه سیستم را از حالت 2 به حالت 1 در امتداد B ببرید، مسیر برگشت پذیر دیگری C را در نظر بگیرید. سپس برای این چرخه 1-A-2-C-1، نابرابری Clausius را اعمال کنید:
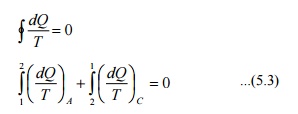
مقایسه 5.2 و 5.3
از این رو، می توان نتیجه گرفت که کمیت تابع نقطه ای است، مستقل از مسیر طی شده. بنابراین یک ویژگی سیستم است. با استفاده از نماد S برای آنتروپی می توانیم بنویسیم
پس از ادغام ما دریافت می کنیم

برای یک فرآیند برگشت پذیر.
تغییر آنتروپی برای یک فرآیند برگشت ناپذیر
رابطه بین تغییر آنتروپی و انتقال حرارت در سراسر مرز در طول فرآیندهای برگشت ناپذیر را می توان با یک چرخه ساده متشکل از دو فرآیند نشان داد که یکی از آنها به صورت داخلی برگشت پذیر و دیگری غیرقابل برگشت است، همانطور که در شکل 5.3 نشان داده شده است. نابرابری Clausius اعمال شده برای این چرخه برگشت ناپذیر را می توان به صورت نوشتاری نوشت
از آنجایی که فرآیند B به صورت داخلی قابل برگشت است، این فرآیند می تواند معکوس شود و بنابراین
همانطور که در معادله 5.5 تعریف شده است، از آنجایی که فرآیند B برگشت پذیر است، انتگرال سمت چپ را می توان به صورت بیان کرد.
دما - نمودار آنتروپی
در نمودار Ts نواری با ضخامت ds با ارتفاع متوسط T همانطور که در شکل 5.4 نشان داده شده است در نظر بگیرید. سپس Tds مساحت نوار را می دهد.
برای یک فرآیند برگشت پذیر انتقال حرارت عنصری
dQ =Tds =مساحت نوار
برای به دست آوردن انتقال حرارت کل باید معادله فوق را بین حدود 1 و 2 ادغام کرد، به طوری که،
این معادل مساحت زیر یک منحنی است که فرآیند را در نمودار TS نشان می دهد همانطور که در شکل 5.4 نشان داده شده است.
توجه: – برای یک فرآیند همدما S 2 -S 1 = .
– برای فرآیند برگشت پذیر آدیاباتیک S 2 -S 1 =0.
تغییر در آنتروپی
الف) جامدات و مایعات
تغییر در آنتروپی
جایی که dq =du + pdv
برای جامدات و مایعات
پی دی وی = 0
جایی که c- گرمای ویژه است
ب) برای گازهای ایده آل تغییر آنتروپی
جایگزین کردن
du =C v dT
پس از ادغام دریافت می کنیم
جایگزینی dh =C p dT
و ما دریافت می کنیم
پس از ادغام
اصل افزایش آنتروپی
استفاده از نابرابری کلازیوس،
برای یک سیستم ایزوله که تحت یک فرآیند قرار می گیرد
سیستمی را در نظر بگیرید که با محیط اطراف خود در تعامل است. اجازه دهید سیستم و محیط اطراف آن در یک مرز قرار گیرند که یک سیستم ایزوله را تشکیل می دهد. از آنجایی که همه واکنش ها در سیستم ترکیبی انجام می شود، می توانیم بیان کنیم
یا
هرگاه فرآیندی رخ دهد، آنتروپی جهان (سیستم به اضافه محیط اطراف) در صورت برگشت ناپذیری افزایش می یابد و اگر برگشت پذیر باشد ثابت می ماند. از آنجایی که همه فرآیندها در عمل برگشت ناپذیر هستند، آنتروپی جهان همیشه افزایش می یابد
به عنوان مثال، ( Ds) جهان > 0
این به عنوان اصل افزایش آنتروپی شناخته می شود.
راندمان آدیاباتیک کمپرسورها و توربین ها
در کمپرسورها و توربینهای جریان ثابت فرآیند آدیاباتیک برگشتپذیر فرآیند ایدهآل در نظر گرفته میشود. اما به دلیل برگشت ناپذیری های ناشی از اصطکاک بین سیال جاری و پروانه ها، این فرآیند اگرچه آدیاباتیک است، برگشت پذیر نیست. درصد انحراف این فرآیند از فرآیند ایده آل بر حسب بازده آدیاباتیک بیان می شود.
الف) کمپرسورها:
از آنجایی که کمپرسورها دستگاه هایی هستند که کار مصرفی دارند، کار واقعی مورد نیاز بیش از کار ایده آل است. برای کمپرسورهایی که گازهای ایده آل را مدیریت می کنند
ب) توربین ها:
در توربین به دلیل برگشت ناپذیری، خروجی کار واقعی کمتر از کار ایزنتروپیک است.
مشکلات حل شده
مشکل: 5.1 جسمی در دمای 200 درجه سانتیگراد تحت یک فرآیند همدما برگشت پذیر قرار می گیرد. انرژی گرمایی حذف شده در این فرآیند 7875 J است. تغییر آنتروپی بدن را تعیین کنید.

نظر: با حذف گرما از سیستم، آنتروپی کاهش می یابد.
مشکل: 5.2 جرم 5 کیلوگرمی آب مایع از 100 درجه سانتیگراد تا 20 درجه سانتیگراد خنک می شود. تغییر آنتروپی را تعیین کنید.
سیستم: سیستم بسته

نظر : با حذف گرما از سیستم، آنتروپی کاهش می یابد.
مشکل: 5.3 هوا به صورت همدما از 100 کیلو پاسکال تا 800 کیلو پاسکال فشرده می شود. تغییر درآنتروپی خاص هوا را تعیین کنید.
سیستم : بسته/باز
شناخته شده : p 1 =100 کیلو پاسکال
p2 = 800 کیلو پاسکال
برای پیدا کردن : DS - تغییر در آنتروپی خاص
تجزیه و تحلیل : DS = -R ln [از آنجایی که فرآیند همدما است]
=0.287 -x ln
= 0.597 -kJ/kgK.
مشکل: 5.4 جرم 5 کیلوگرمی هوا از 90 کیلو پاسکال، 32 درجه سانتیگراد تا 600 کیلو پاسکال درفرآیند پلی تروپیک فشرده می شود، pV 1.3=ثابت. آنتروپی تغییر را تعیین کنید.
سیستم : بسته / باز
شناخته شده : p1 = 90کیلو پاسکال
T 1 =32 o C =305 K
p 2 =600 کیلو پاسکال
متر =5 کیلوگرم
فرآیند : pV 1.3 =ثابت
برای پیدا کردن : DS - تغییر در آنتروپی
تجزیه و تحلیل : S 2 -S 1=m
جایی که T 2 =T 1
=305
=473 K
\S 2 -S 1 =5
=0.517 کیلوژول/کیلو.
نظر: نسبت Cp و Cv برای هوا برابر 1.4 است. بنابراین شاخص پلی تروپیک n -1.3 (<1.4) نشان می دهد که مقداری گرما از سیستم حذف می شود که منجر به آنتروپی منفی می شود.
مشکل: 5.5 یک ظرف عایق صلب 5 کیلوگرم گاز ایده آل را در خود جای می دهد. گاز را طوری هم می زنند که حالت آناز 5 کیلو پاسکال و 300 کیلو پاسکال به 15 کیلو پاسکال تغییر کند. با فرض C p=1.0 kJ/kgK وg =1.4، تغییر آنتروپی سیستم را تعیین کنید.
سیستم : بسته
فرآیند : حجم ثابت از زمانی که گاز در یک ظرف سفت و سخت به هم زده می شود

3.922 kJ /K =
نظر : اگرچه این فرآیند آدیاباتیک است، اما ایزنتروپیک نیست زیرا فرآیند هم زدن یک فرآیند برگشت ناپذیر است.
مشکل: 5.6 یک ظرف صلب عایق شده به دو محفظه با حجم مساوی تقسیم می شود. یک محفظهحاوی هوا با 500 کلوین و 2 مگاپاسکال است. اتاق دیگر تخلیه می شود. اگر دو محفظه d به هم متصل شوند، تغییر آنتروپی چقدر خواهد بود؟
سیستم : سیستم بسته
فرآیند : گسترش بدون مقاومت

=0.199 kJ/kgK
نظر : اگرچه فرآیند آدیاباتیک است، آنتروپی با درگیر شدن فرآیند افزایش می یابد
گسترش بدون مقاومت یک فرآیند برگشت ناپذیر است. این واقعیت را نیز ثابت می کند
مشکل: 5.7 یک محفظه آدیاباتیک به دو بخش مساوی تقسیم می شود. در یک طرفاکسیژن در 860 کیلو پاسکال و 14 درجه سانتیگراد وجود دارد. در طرف دیگر نیز اکسیژن وجود دارد اما در 100 کیلو پاسکال و 14 درجه سانتیگراد. محفظه عایق و دارای حجم 7500 سی سی است. پارتیشن به طور ناگهانی حذف می شود. فشار نهایی و تغییر آنتروپی جهان را تعیین کنید.

مشکل: 5.8 یک سیستم بسته از طریق یک چرخه متشکل از چهار فرآیند برگشت پذیر انجام می شود. جزئیاتفرآیندها در زیر ذکر شده است. اگر سیستم 100 سیکل در دقیقه اجرا می کند، توان توسعه یافته را تعیین کنید.


منبع
https://www.brainkart.com/article/Entropy_5460/
 در این وبلاگ به ریاضیات و کاربردهای آن و تحقیقات در آنها پرداخته می شود. مطالب در این وبلاگ ترجمه سطحی و اولیه است و کامل نیست.در صورتی سوال یا نظری در زمینه ریاضیات دارید مطرح نمایید .در صورت امکان به آن می پردازم. من دوست دارم برای یافتن پاسخ به سوالات و حل پروژه های علمی با دیگران همکاری نمایم.در صورتی که شما هم بامن هم عقیده هستید با من تماس بگیرید.
در این وبلاگ به ریاضیات و کاربردهای آن و تحقیقات در آنها پرداخته می شود. مطالب در این وبلاگ ترجمه سطحی و اولیه است و کامل نیست.در صورتی سوال یا نظری در زمینه ریاضیات دارید مطرح نمایید .در صورت امکان به آن می پردازم. من دوست دارم برای یافتن پاسخ به سوالات و حل پروژه های علمی با دیگران همکاری نمایم.در صورتی که شما هم بامن هم عقیده هستید با من تماس بگیرید.